
生物相容性 目錄
醫療器材 生物相容性試驗 ISO 10993
生物相容性測試的目的就是要確保人體在接觸到材料後,材質不會釋放有毒物質,造成局部或全身性細胞毒性、致癌性及生殖毒性,人體在接觸到材料後不會引起發炎反應、免疫反應、毒性反應、血栓形成反應等危害。
衛福部 TFDA 參照廣為國際衛生主管機關、學界和業界所使用的 ISO 10993 系列為規範標準,而醫療器材管理辦法主要參考美國 FDA,將醫療器材依據風險程度,分成下列三種等級:
第一等級:低風險性
第二等級:中風險性
第三等級:高風險性
只有第三等級和部分的第二等級產品上市前需執行臨床前試驗,需要提供相關資料暨文獻,例如由符合優良實驗室操作規範 (GLP) 的實驗室提供臨床前試驗結果報告及非臨床安全性評估(生物相容性)以證明產品之安全性及品質。
ISO 10993-1:2018新版 醫材生物相容性分類表
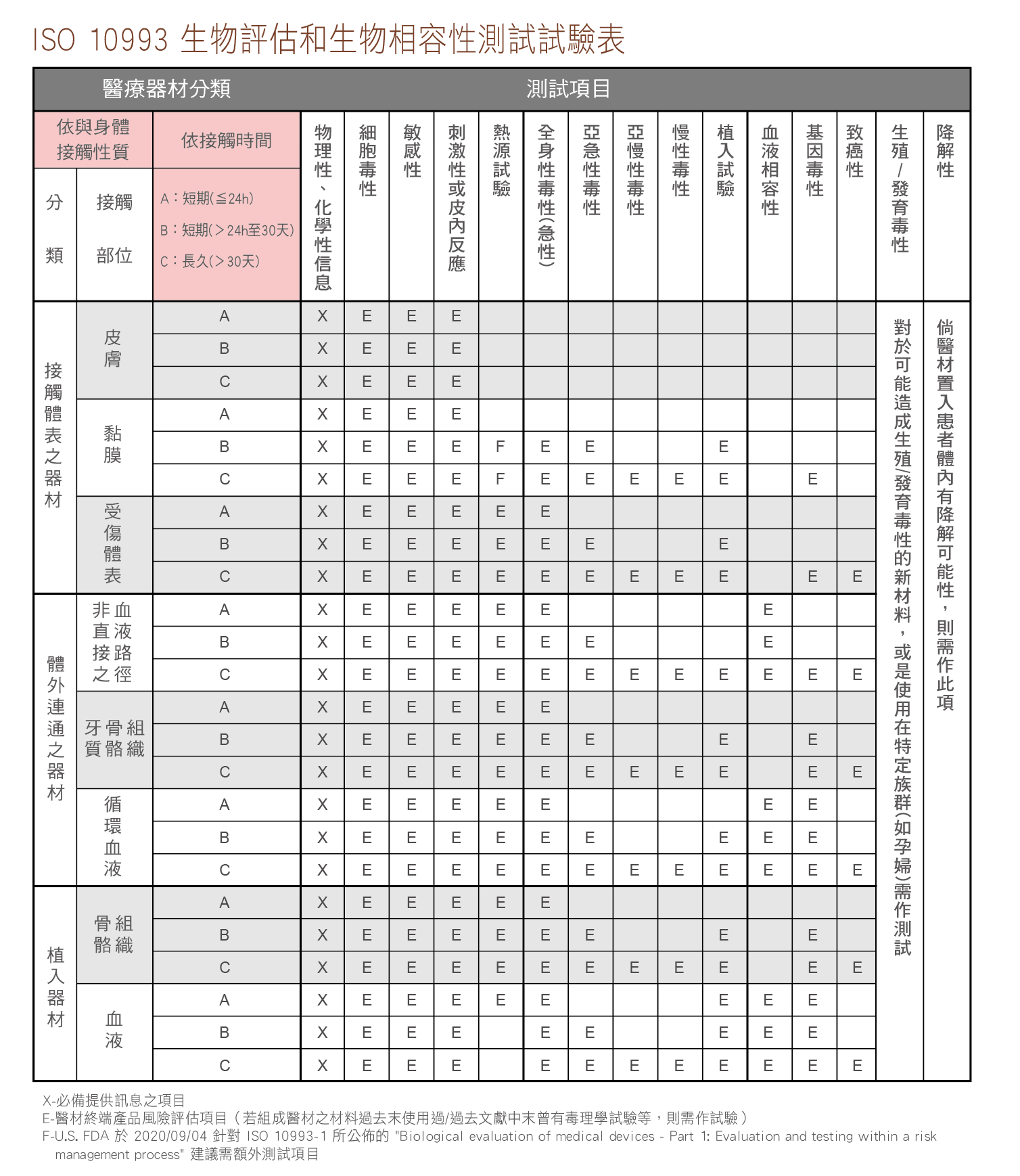
生物相容性試驗介紹
-
細胞毒性試驗 Cytotoxicity Test
細胞受有毒物質刺激時,會引起細胞整體型態改變、空泡化、剝離化、細胞溶解及細胞膜完整性發生改變,甚至引起細胞死亡等現象,藉由活細胞能將 MTT 黃色化合物,作用於細胞線粒體中的呼吸鏈,在琥珀酸脫氫酶,生成藍色的 formazan 結晶,偵測吸收光判斷細胞存活。
-
皮膚敏感性試驗 Skin Sensitisation Test
評估醫療器材、物質上有否會引發接觸性過敏反應與遲發型過敏反應 (Type IV) 之成分,為最靈敏之敏感性試驗。測試物經過萃取後,將佐劑 (Adjuvant) 與萃取液做適當混合,注射至天竺鼠之皮內,放大可能的過敏反應,觀察是否存有潛在致敏性。
試驗方法:極大化敏感性試驗、密封式貼片試驗
參照規範:
-
ISO 10993-10 Tests for skin sensitization
-
OECD #406 Skin sensitisation
-
皮膚刺激性試驗 Skin Irritation Test
評估醫療器材、物質成分內有否會引發皮膚刺激性之成分。測試物直接或經過萃取後,以貼片吸取萃取液,貼附於大白兔之皮膚表層,觀察是否存有潛在刺激性。
參照規範:
- ISO 10993-23 Tests for irritation
- OECD #404 Acute dermal irritation/corrosion
-
皮內刺激性試驗 Intracutaneous Irritation Test
評估醫療器材、物質成分內有否會引發皮內刺激性之成分。測試物經過萃取後,將萃取液注射至大白兔之皮內,觀察是否存有潛在刺激性。
參照規範:ISO 10993-23 Tests for irritation
-
眼睛刺激性試驗 Eye Irritation Test
評估醫療器材、物質成分內有否會引發眼球刺激性之成分。測試物經過萃取後,將萃取液滴入大白兔之眼球,觀察其對眼球(角膜、結膜、虹膜)是否存有潛在刺激性。
參照規範:
- ISO 10993-23 Tests for irritation
- OECD #405 Acute eye irritation/corrosion
-
系統毒性試驗 Acute Systemic Toxicity Test
評估醫療器材、物質成分內,藉由受試動物單次短期接觸醫療器材或其萃取物,評估其潛在危害效應。
參照規範:ISO10993-11 Tests for systemic toxicity
-
熱原試驗 Pyrogen Test
評估醫療器材、物質成分內有否存在熱原之成分。測試物經過萃取後,將萃取液經由耳靜脈注射至大白兔體內,之後觀察其體溫之變化。
參照規範:USP 151 Pyrogen Test
-
內毒素試驗 Endotoxin Test
內毒素是一種由革蘭氏陰性菌所產生的毒素,是引起人體發熱反應的熱原中最常見的一種,常見比濁法與呈色法計算內毒素。當比濁法試劑碰到細菌內毒素會呈現凝集混濁現象;呈色法試劑碰到細菌內毒素,試劑中的 Boc-Leu-Gly-Arg-pNA可被凝集酵素切出 p-Nitroaniline,呈現黃色反應,再以標準曲線計算濃度。
-
植入試驗 Implantation Test
評估醫療器材、物質成分內有否會引發局部反應之成分。將測試物植入大白兔體內適當之部位(皮下、肌肉、骨骼等),觀察其臨床生理狀況與顯微鏡觀察組織病理切片分析,評估是否存有潛在不良反應。
參照規範:ISO 10993-6 Tests for local effects after implantation
-
溶血試驗 Hemolysis Test
溶血的定義為血紅素由破壞或部分受損但仍保持細胞膜完整的紅血球所釋放出來。一般以體外試驗來評估紅血球之損傷,試驗方法包括:
- 直接接觸法:檢測因物理性作用力(如:滲透壓改變)或化學物質與紅血球交互作用而導致的溶血。
- 萃取法:檢測因試驗物質萃取液所導致的溶血。使用使用市售血紅素檢測套組偵測血紅素。

你必須登入才能發表留言。